JAFC 南宁学院-生淀粉降解酶的发现、表达、改造及应用:现状与展望
2025年11月11日,来自南宁学院的Ting Zhang等人在Journal of Agricultural and Food Chemistry上发表了一篇题为Discovery, Expression, Modification, and Application of Raw Starch-Degrading Enzymes: Current Status and Future Perspectives的综述性论文。

Abstract
淀粉是一种储量丰富、成本低廉的可再生碳水化合物,但传统的酶法生物精炼需要高能耗的液化和糖化过程,降低了经济可行性。生淀粉降解酶能够在低温下直接水解生淀粉颗粒,但天然形式的酶存在催化效率低、稳定性差和产量有限的问题。本文综述了近年来RSDEs在发现、表达、改造及应用方面的研究进展。讨论了通过遗传调控关键因子(特别是调控淀粉酶基因网络的转录因子)来增强RSDEs表达的策略。随后,详细介绍了包括蛋白质工程和遗传修饰在内的分子改造方法,以提升RSDEs的性能和产量。此外,重点介绍了用于RSDEs规模化生产和应用的高产工程菌株的开发。最后,展望了下一代RSDEs的未来发展方向。本综述为RSDEs的工业化应用提供了全面基础,并为开发高性能酶和稳健生产平台提供了战略性见解。
Introduction
淀粉是一种丰富的碳水化合物,广泛应用于发酵工业以生产生物燃料(如生物乙醇)、酒精饮料、有机酸和氨基酸。它还在食品、造纸、制药和纺织等领域有着广泛的应用。作为一种可再生、可持续的能源,生物乙醇有助于减轻环境污染和应对能源危机,预计到2040年全球能源需求将增长28%。许多国家计划到2030年将20-30%的生物乙醇掺混到汽油中。
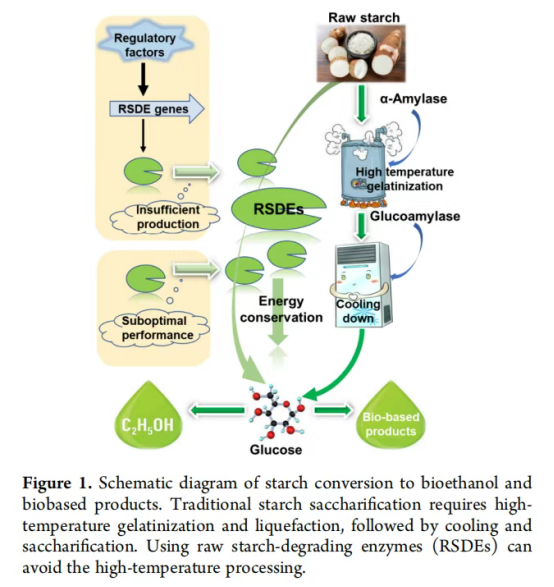
传统的淀粉加工通常采用耐热α-淀粉酶在95至105°C的高温下进行液化。这种方法导致能耗高、工艺复杂、生产成本增加。在糊化温度以下水解淀粉可降低成本30-40%。能够在糊化温度以下有效且直接水解生淀粉颗粒的淀粉酶(此过程称为"冷加工")通常被称为生淀粉降解酶。本文中,使用缩写RSDA和RSDG分别指代两种主要的RSDEs,即生淀粉降解淀粉酶和生淀粉降解葡萄糖淀粉酶。它们对天然生淀粉颗粒的高活性是由表面结合、酶结构和底物特征共同决定的。当应用于淀粉糖工业时,这种能力简化了生产过程,提高了效率,并降低了能耗(图1)。Robertson等发现,在生物乙醇生产中使用RSDG可降低能耗10-20%。"冷加工"方法省去了高温糊化步骤,从而降低了生物乙醇等淀粉基产品的生产成本。RSDG因其广泛的商业用途,包括生产淀粉基糖、多孔淀粉和高葡萄糖浆等,在各个行业备受关注。
目前,RSDEs主要来源于真菌(如曲霉属、根霉属、青霉属)和细菌(如芽孢杆菌属)。这些来源具有生产成本低、一致性好、生产周期短、易于工艺优化等优点。然而,挑战依然存在,包括来源有限、产量低、催化效率不足和反应温度高等问题。此外,不同来源的RSDEs在催化活性和热稳定性方面存在显著差异。由于RSDEs在自然环境中主要由丝状真菌分泌,其生产和应用受到调控因子和培养条件的显著影响¹¹。因此,开发具有优良特性的RSDEs以及合适的生产菌株将有助于其在淀粉加工中的应用。
随着基因工程和蛋白质工程等现代生物技术的进步,RSDEs已从单纯的筛选发展到通过酶的设计与优化来增强其热稳定性和催化效率。迫切需要通过结构模拟和分子修饰来提升RSDEs的性能,并实现重组酶的高效合成,同时理解RSDEs表达的调控机制。
本文综述了近年来RSDEs(重点关注RSDAs和RSDGs)在发现、表达、改造及应用方面的研究进展。讨论了通过遗传操作调控因子(特别是控制淀粉酶相关基因表达的转录因子)来提高RSDEs表达的策略。随后,我们详细介绍了分子改造方法——主要包括蛋白质工程(如分子间作用力和表面电荷优化、定向进化和定点突变、以及通过遗传操作进行的N/C端和SBD工程)和遗传修饰(如用于转录增强的启动子工程、密码子优化和多拷贝基因整合、用于分泌或稳定性的融合蛋白策略)——以提升RSDEs的性能和产量。此外,总结了通过基因工程构建的用于规模化生产RSDEs的高产工程菌株。最后,对RSDEs的未来发展提出了几点展望。本综述为RSDEs的工业化规模应用提供了全面基础,并为开发高性能酶和稳健生产平台提供了战略性指导。
生淀粉与生淀粉降解酶
生淀粉是一种天然、环保、廉价、可持续且可再生的碳水化合物聚合物,来源于谷物、豆类以及多种植物的根和种子。它是人类和动物的重要营养来源,也是一种重要的工业原料,预计到2025年全球产量将达到1.565亿吨。考虑到物种和品种的差异、淀粉颗粒与其他组分结合方式的区别以及估算方法的不同,不同来源的淀粉产量存在差异。淀粉颗粒主要含有两种α-葡聚糖:直链淀粉,一种主要由α-1,4连接的葡萄糖组成的线性链,带有少量α-1,6分支;以及支链淀粉,一种高度分支的聚合物,约含5%的α-1,6连接。淀粉根据直链淀粉含量分为蜡质(0-8%)、普通(20-40%)和高直链淀粉(50-90%)类型。此外,直链淀粉极大地影响淀粉的性质和用途,测定其含量对于食品加工和质量控制至关重要。
不同的淀粉颗粒表现出"A"型、"B"型或"C"型的广角X射线衍射图样。例如,蜡质和普通淀粉呈现典型的"A"型图样,而高直链淀粉则显示特征性的"B"型图样。研究表明,"B"型结晶中的支链淀粉组分通常比"A"型淀粉中的支链淀粉具有更长的链长,并且支链淀粉的有序排列增强了淀粉颗粒的结晶特性,而直链淀粉比例较高的淀粉结晶度往往较低。通常,天然淀粉是半结晶的。影响结晶类型的因素包括生长温度、是否存在醇或脂肪酸,以及支链淀粉的链长。此外,淀粉的化学和矿物质含量受植物来源和所用提取方法的影响。根据所使用的酶和水解条件,颗粒内的晶体结构和有序度也会相应地发生改变。
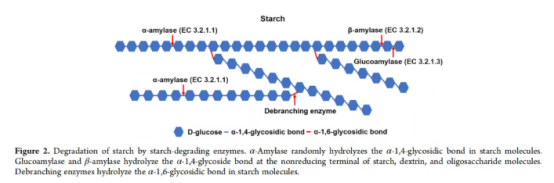
淀粉糖工业中的淀粉水解包含糊化、液化、糖化和脱支等多个过程,需要三大类酶。(1)液化酶:α-淀粉酶,它能分解α-1,4-糖苷键。此过程降低粘度并释放α-糊精、寡糖和葡萄糖。(2)糖化酶:包括葡萄糖淀粉酶、β-淀粉酶和α-葡萄糖苷酶。它们进一步水解淀粉以产生麦芽糖和葡萄糖。葡萄糖淀粉酶能从非还原端依次切下单分子β-D-葡萄糖,也能缓慢作用于α-1,6分支点。β-淀粉酶,也称为麦芽糖苷酶,与葡萄糖淀粉酶协同水解淀粉、糊精和寡糖中的α-1,4-糖苷键,生成麦芽糖和葡萄糖。随后,α-葡萄糖苷酶将麦芽糖分解为葡萄糖。糖化酶产生的主要水解产物是葡萄糖、麦芽糖、β-极限糊精和其他小分子糖。(3)脱支酶:包括普鲁兰酶、异淀粉酶和淀粉普鲁兰酶。这些酶特异性地作用于分支淀粉中的α-1,6-糖苷键,释放寡糖、麦芽三糖、麦芽糖和葡萄糖。其中,普鲁兰酶和异淀粉酶分别靶向较低和较高分子量的糊精。淀粉普鲁兰酶的独特之处在于它能同时水解α-1,4-和α-1,6-糖苷键。此外,来自辅助活性家族13的新型淀粉活性裂解性多糖单加氧酶已被证明能通过引入氧化性切割,在淀粉多糖中产生新的链末端,从而加速后续的水解降解。
淀粉降解酶系统的作用机制如图2所示。简而言之,线性的直链淀粉可以通过液化和糖化酶几乎完全分解为葡萄糖。相比之下,有分支的支链淀粉需要三类酶的协同作用:首先由液化和脱支酶水解成不同长度的寡糖链,随后由糖化酶分解为葡萄糖。
约10%的淀粉降解酶能够吸附并水解生淀粉颗粒;这种能力通常由非催化性的淀粉结合结构域介导,尽管也有极少数不含SBD的RSDEs被报道。基于序列的分析已将SBDs分类到碳水化合物结合模块家族中;截至2025年10月,在已建立的107个CBM家族中,有15个——CBM20、21、25、26、34、41、45、48、53、58、68、69、74、82和83——已被证实含有SBDs(Janecek等,2019;https://www.cazy.org/Carbohydrate-Binding-Modules.html)。Janecek等(2019)已汇编了每个含SBD的CBM家族的基本特征,在此不再赘述。除了单纯的结合外,一些SBDs还能主动破坏淀粉结构:例如,CBM20促进直链淀粉中平行双螺旋的破坏,而CBM74则扩大淀粉颗粒中的孔隙,从而为随后的酶促攻击做好准备。有趣的是,CBMs既可以促进也可以阻碍生淀粉的水解,这种双重行为根植于界面酶催化的Sabatier原理所预测的双相结合-活性关系。根据该原理,最佳的催化活性在中等酶-底物结合强度下实现,而过弱或过强的相互作用都会损害整体效率。
生淀粉降解酶的发现
RSDEs广泛分布于植物、动物和微生物中;然而,由于其遗传多样性和稳健的催化特性,微生物来源的RSDEs是当前生物制造的主力。多种菌株,例如分离出的系统发育相关杆菌CS-148,已被证实能在最适条件下高效地将生淀粉水解为葡萄糖,显著提高葡萄糖产量。其他菌株,如棒曲霉和嗜热地芽孢杆菌,也表现出高水解活性,显示出巨大的工业潜力。此外,来自Priestia flexa的三元RSDA在生物乙醇生产中具有应用前景。表1总结了30多种近期被鉴定的RSDAs、RSDGs以及能够水解生小麦、马铃薯、玉米、木薯或西米颗粒淀粉的多酶复合物。
值得注意的是,来自巨大芽孢杆菌NL3的RSDA BmaN1的C末端区域能有效增强酶的生淀粉结合和水解活性。类似地,来自嗜热脂肪地芽孢杆菌的RSDA Gt-amy通过其C末端结构域结合生淀粉,该结构域也有助于维持其热活性和稳定性。然而,来自B. aquimaris MKSC 6.2的截短型BaqAΔC变体在50°C或1.5 M NaCl条件下处理6小时后仍保留≥50%的RSDA活性,表明微小的C末端重构可以在结合强度与增加的稳定性和耐盐性之间进行权衡。总的来说,这些发现凸显了C末端作为一个可调模块,这一"修饰热点"已使得能够快速开发适用于低温、高盐或节能型生淀粉加工的定制生物催化剂。
在过去几年中,研究人员越来越关注极端生境——盐矿、酸性矿山排水系统、高碱性盐湖、垃圾土壤等——并结合宏基因组学、宏转录组学与传统培养方法,系统地挖掘分泌强健RSDEs的微生物菌株。Ying等人成功从盐渍土壤中分离出一株耐盐细菌,命名为Halolactibacillus sp. SK71,其产生的胞外RSDG可被纯化并用于水解生玉米淀粉,随后利用酿酒酵母进行生物乙醇生产⁴¹。然而,目前普遍认为,分离位点的物理化学条件并不一定决定所产酶的最适pH或温度:酸性位点的分离物可能偏好碱性条件,反之亦然³⁷。由于这些适应性是遗传编码的,它们可以通过结构域改组或在嗜温宿主中表达进行转移,提供了即插即用的模块,缩短了从发现到商业应用的路径。因此,鼓励后续研究将BLAST、UniProt和AlphaFold3分析与严格的生化表征相结合;这种数据驱动的流程可以揭示不断扩展的酶世界中酶的进化轨迹、结构特征和功能差异,从而指导下一代生物催化剂的靶向发现⁴²。总之,极端微生物是RSDEs的重要资源库,这些酶在严苛的工业条件下仍能保持活性,而计算机挖掘与实验验证的迭代循环将加速其从实验室走向生物工艺的转化。
生淀粉降解酶的异源表达
在生物技术进步的推动下,微生物细胞工厂中的异源表达现在能够实现高性能RSDEs的工业化规模生产,克服了天然产量低和批次间差异的问题,同时提供了克/升级的产量、精确的糖基化控制以及用于进一步蛋白质工程的清洁背景。研究表明,来自不同微生物的RSDEs表现出强劲的生淀粉消化活性。例如,来自赤子爱胜蚓的RSDAs Ef-Amy I和Ef-Amy II在毕赤酵母中表达,它们是冷适应的,适用于同步糖化发酵过程。来自巨大芽孢杆菌NL3的RSDA BmaN2在大肠杆菌中表达,对颗粒小麦具有高比活力。此外,来自深海细菌Pontibacillus sp. ZY的RSDA AmyZ1在大肠杆菌中表达,能有效水解多种来源的生淀粉,表明其工业应用潜力。来自黄曲霉NSH9的RSDG GA2和来自烟曲霉A1163的RSDG在毕赤酵母中也显示出有希望的结果,特别是在低温和高淀粉浓度的发酵过程中。有趣的是,在毕赤酵母中表达的烟曲霉A1163 RSDG,在将生玉米淀粉转化为葡萄糖方面显示出比在大肠杆菌中表达时更好的水解能力。
在本实验室,来自草酸青霉GXU20的RSDG编码基因PoGA15A在毕赤酵母中成功表达。重组RSDG PoGA15A在40°C条件下与α-淀粉酶联合使用时,能够高效快速地水解生玉米淀粉和生木薯淀粉。因此,当150 g/L的生木薯淀粉同步糖化发酵36小时后,该工艺产生的乙醇浓度为57.0 g/L,发酵效率达到93.5%。总的来说,如表1所概述,这些RSDEs在淀粉加工和生物乙醇生产中具有重要价值。
用于RSDEs异源表达的三种主流宿主——大肠杆菌、毕赤酵母和枯草芽孢杆菌——在产量、翻译后修饰、分泌效率、成本和操作复杂性方面存在显著差异。(1)大肠杆菌提供了最快、最经济的途径,其可溶的胞内表达可产生高比活力。然而,显著的密码子偏好性、缺乏糖基化以及包涵体的形成限制了其在结构-功能研究、快速筛选或构建首轮突变文库中的应用。(2)毕赤酵母提供真核生物的高甘露糖型糖基化、强大的分泌能力以及几乎无背景的上清液,在高密度补料分批培养中常规产量可达10-30 g·L⁻¹。甲醇诱导需要安全/环境控制,且过度糖基化可能降低比活力。因此,该平台更适用于能耐受聚糖修饰的分泌型RSDEs的工业化规模生产。(3)枯草芽孢杆菌是一种食品级的GRAS(一般认为安全)微生物,无内毒素,能在短发酵周期内将酶直接分泌到培养基中。其产量通常低于毕赤酵母,且质粒不稳定和内源蛋白酶问题需要仔细管理;尽管如此,该系统非常适合食品级或饲料级酶制剂以及要求零内毒素的应用。总之,大肠杆菌应选择用于结构-功能分析和高通量筛选;毕赤酵母用于克级分泌生产和放大;而当食品级安全和快速工艺转化至关重要时,应选择枯草芽孢杆菌。
然而,宿主特异性的瓶颈仍然阻碍着RSDEs的规模化、高质量生产。新兴的解决方案——包括启动子和载体工程、密码子优化、分子伴侣共表达、糖基化与分泌途径重构、发酵优化以及机器学习引导的高通量筛选——现在正在细菌和真核表达平台中系统地解决这些局限性。此外,信号肽和转运组分的定向进化正在加速创建分泌优势型宿主菌株,而人工智能驱动的设计-构建-测试-学习循环进一步缩短了从基因到吨级酶产品的开发时间。
调控因子对淀粉酶基因表达的调控
调控编码淀粉酶的基因表达正受到越来越多的关注,当前研究主要集中在转录调控上(图3)。众多转录因子、NADH激酶、丝裂原活化蛋白激酶和其他激酶、G蛋白偶联通路相关因子以及甲基转移酶Mtr23B已被鉴定为关键的正调控因子。相反,包括转录因子和SWI/SNF复合体组分在内的几种蛋白质被发现作为负调控因子起作用。
(1)调控淀粉酶基因表达的正向转录因子
Zn2Cys6型转录因子AmyR,对于曲霉属和青霉属物种中响应麦芽糖、异麦芽糖和淀粉诱导的淀粉酶基因表达至关重要。值得注意的是,AmyR的激活依赖于Zn2Cys6型转录因子MalR的预先激活,且与其细胞内定位无关。Hu等人近期发现,草酸青霉中的组蛋白乙酰转移酶复合物Hat1-Hat2作为AmyR的转录辅因子,调控淀粉酶基因的转录。具体而言,AmyR结合到关键淀粉酶基因的上游区域,招募Hat1-Hat2复合物,促进组蛋白H4K12的乙酰化,同时招募共抑制因子Tup1-Cyc8以稳定正常转录水平。相反,Hat1的缺失会破坏这一过程,释放转录"刹车"(图3A)。
此外,米曲霉中的碱性螺旋-环-螺旋型转录因子DevR可能与amyR启动子相互作用,调控amyR表达并影响其他淀粉酶相关基因。而且,AmyR负调控蛋白酶调控因子PrtT(也是一种Zn2Cys6型转录因子)及其靶基因,包括酸性蛋白酶基因pepA。PrtT可能与AmyR竞争,从而抑制蛋白酶和淀粉酶基因的表达。进一步的研究表明,C2H2型转录因子CxrB和GATA型转录因子NsdD都正调控RSDE的产生和PoxGA15A的表达。CxrB通过调控amyR表达间接影响主要淀粉酶基因的转录。相比之下,NsdD直接调控PoxGA15A和amyR的表达。与原始菌株相比,nsdD的缺失导致RSDE活性降低52.6%至78.8%(图3A)。
在草酸青霉HP7-1菌株中,陆续鉴定出五个特异性调控RSDE产生的转录因子,命名为RsrA-E。其中,SANT/Myb型转录因子RsrA在Y1127和Y1170位点的磷酸化,以及它对辅因子Med31(中介体复合物亚基)的招募,对于增强关键RSDG基因PoxGA15A和其他淀粉酶相关基因的表达,从而提高RSDE产量至关重要。Ning等人近期发现了一个涉及RsrA、Zn2Cys6型转录因子RsrB和C2H2型转录因子RsrC的转录级联,它们正调控RSDE的生物合成。值得注意的是,RsrC直接结合到rsrA基因的启动子区域以增强其表达和RSDE的产生。随后,RsrA刺激rsrB基因的转录,而RsrB¹⁶⁵⁻²⁷¹蛋白则结合到PoxGA15A启动子的5'-TCGATCAGGCACGCC-3' DNA序列上。此外,碱性亮氨酸拉链型转录因子RsrD和Zn2Cys6型转录因子RsrE间接调控RSDE基因的表达和产量,同时在转录水平上彼此也产生直接影响(图3A)。
此外,Zn2Cys6型转录因子Art1对于淀粉水解至关重要,其在镰孢菌属物种中的缺失突变体表现出淀粉酶基因表达降低,从而影响淀粉水解和霉菌毒素的产生。这些发现表明这些转录因子在真菌的生长和代谢中发挥着多重作用。有趣的是,C2H2型转录因子FlbC,主要以其在调节分生孢子发育中的作用而闻名,在固态培养条件下也调控葡萄糖淀粉酶基因glaB和酸性蛋白酶基因pepA。然而,它不调控耐酸α-淀粉酶基因(图3A)。
(2)调控淀粉酶基因表达的负向转录因子
相反,CreA,一种参与碳分解代谢物阻遏的关键C2H2型转录因子,可能在葡萄糖存在下通过招募共抑制因子复合物Tup1-Cyc8来抑制与生物技术相关的酶基因的表达。有趣的是,S319位点的磷酸化对于CreA的降解和酶活性的诱导至关重要,而S262、S268和T308位点则影响CreA的积累和功能。类似地,BrlA,另一种C2H2型转录因子,不仅在草酸青霉中正调控分生孢子形成,而且负调控主要纤维素酶和淀粉酶基因的表达。一个HMG-box蛋白PoxHmbB,在可溶性玉米淀粉诱导下负调控淀粉酶活性,但在Avicel诱导下正调控纤维素酶活性(图3A)。
在报告中,发现一个非CCR相关的Zn2Cys6型转录因子CxrC负调控RSDE的产生,ΔcxrC突变体的产量比Δku70突变体高出1.5至1.8倍。与CxrC多聚体形成相关的关键区域CxrC¹²⁻²⁸⁸和保守基序LPSVRSLLTP(第65-74位)对其调控功能至关重要。此外,在Talaromyces pinophilus 1-95中与CxrC同源性最高的Zn2Cys6型转录因子TP05746,通过直接影响淀粉酶及其调控基因的表达来调控真菌淀粉酶的生物合成。重要的是,ΔTP05746突变体中RSDE的产量显著增加(图3A)。
总体而言,这些研究强调了真菌淀粉酶的产生受多种转录因子和辅助蛋白的调控。未来的研究应聚焦于这些转录因子之间的相互作用和调控网络,以更深入地理解这些复杂机制,并开发新的调控工具以提高生物生产效率。
(3)调控淀粉酶基因表达的其他调控因子
除了转录因子外,多种调控因子也参与调节淀粉酶基因的表达。这些因子主要参与不同的信号通路,例如NADPH水平调节、激酶信号通路和G蛋白-cAMP信号通路(图3B)。它们在响应环境信号和代谢状态时,对调节淀粉酶基因的表达水平起着关键作用,确保淀粉酶的产生被精细调控以实现最佳的细胞功能。
首先,研究表明,低NADPH可用性会限制葡萄糖淀粉酶的过量生产。NADH激酶,作为唯一负责产生NADP⁺/H的酶,对于调节细胞内NADP⁺/H水平以及依赖NADP⁺/H的生物合成途径至关重要。过表达特定的NADH激酶基因,如AN03、AN14和AN17,以及NADP依赖的苹果酸酶基因maeA,可以显著增加NADPH库,导致黑曲霉中葡萄糖淀粉酶活性提升50-90%(图3B)。
其次,激酶PoxMK1和PoxMKK1对于调控草酸青霉中Amy15A的表达和RSDE的产生至关重要,尤其是在深层发酵和固态发酵环境中。酪蛋白激酶CK2的两个调控亚基CK2B1和CK2B2,正向调控淀粉酶的产生以及amyR和Amy15A的表达,同时抑制阻遏蛋白CreA。此外,已发现糖原合成酶激酶POGSK-3β能正向调控RSDE的产生和Amy15A的表达,目前正在进行进一步研究以探索其潜在机制(图3B)。
第三,G蛋白偶联的cAMP信号通路对于调控草酸青霉中淀粉酶基因的表达至关重要。具体而言,G蛋白α亚基PGA3和γ亚基GNG1通过调节cAMP介导的amyR转录水平来调控Amy15A/PoxGA15A的表达。此外,G蛋白调节因子——视紫红质抑制蛋白样蛋白PoPlp1,通过调节细胞内cAMP浓度来影响草酸青霉114-2菌株中纤维素酶和淀粉酶基因的转录(图3B)。
此外,染色质重塑复合物在介导转录因子进入受调控基因的特异性结合区域中起着关键作用。SWI/SNF复合物的一个重要成员PoARP9,对于在纤维素酶诱导条件下调控amyR和关键淀粉酶基因的表达至关重要。值得注意的是,甲基转移酶Mtr23B通过与CCAAT结合因子HAP5和来自RSC染色质重塑复合物的ATPase亚基STH1相互作用,显著上调了纤维素酶和淀粉酶基因的转录。Mtr23B的敲除导致amy15A和amy13A基因受到显著抑制(图3B)。

通过分子修饰提升生淀粉降解酶的性能与产量
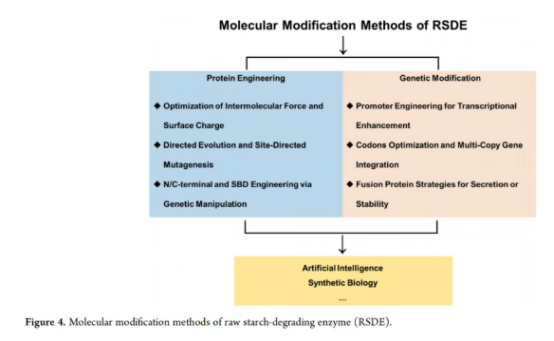
先前的研究已鉴定出一系列能作用于多种植物来源淀粉的RSDEs;然而,它们自然进化的序列在比活力、热稳定性、表达滴度和工艺兼容性方面差异很大。为了弥合天然性能与工业需求之间的差距,研究已从单纯的筛选转向分子定制。蛋白质工程直接重写酶序列以提高催化效率或调节吸附特性,而遗传修饰则提高分泌产量并简化下游回收。这些互补的方法共同构成了分子修饰工具包的核心,并正通过人工智能和合成生物学加速发展(图4)。此外,固定化提供了一种额外的、胞外的稳定化策略。
(1)蛋白质工程策略
酶的热稳定性和酸碱稳定性对于淀粉降解至关重要。蛋白质工程通常用于提高各种工业酶的稳定性,可分为非理性、半理性和理性设计。目前,前两种方法广泛用于工业酶改造。关于具体的修饰策略,读者可参考已发表的综述。在此,重点提供RSDEs蛋白质工程的实例。
分子间作用力与表面电荷的优化许多研究表明,蛋白酶表面氨基酸的分子间作用力和电荷会影响酶内部及其与溶剂的相互作用,以及稳定性和催化活性。目前,主要采用特定的氨基酸插入、替换和删除来调节分子间作用力和表面电荷。一个来自超嗜热真菌Talaromyces leycettanus JCM12802的新型耐热葡萄糖淀粉酶基因TlGa15B被克隆,并在毕赤酵母中表达和表征。通过引入分子间作用力(如二硫键)和优化远离催化中心的电荷相互作用而创建的突变体TlGa15B-GA1和TlGa15B-GA2,表现出增强的催化活性、效率和热稳定性。此外,化学修饰通过增强分子间作用力和优化表面电荷来提升RSDEs的性能。例如,用柠康酸酐对来自Aspergillus carbonarius的RSDG进行酰化修饰,可以提高其催化活性、耐碱性和热稳定性。
定向进化和定点突变定向进化为提高酶性能提供了一条强有力的途径。关键在于突变文库的构建——通过易错PCR、定点饱和突变、DNA改组或相关方法实现,之后通过严格的选择压力结合表型验证来分离阳性克隆。例如,与天然葡萄糖淀粉酶相比,定向进化使来自黑曲霉的突变体THS8和CR2-1的热失活自由能分别提高了5.1和10 kJ·mol⁻¹。
此外,定点突变,例如用丙氨酸替换灵活的甘氨酸残基,用脯氨酸替换丝氨酸,以及替换或删除位于催化结构域表面的延伸环区和高O-糖基化带区,已被证明能有效提高热稳定性。最近,Song等人发现RSDG催化结构域中的N-糖基化修饰影响生淀粉颗粒的降解。通过引入新的N-糖基化位点,他们显著提高了生淀粉的水解效率,糖基化突变体G101S、Q113T和G101S/Q113T对生玉米淀粉的催化活性分别提高了1.19倍、1.21倍和1.22倍。此外,该团队通过饱和突变产生了Q113M突变体,其催化活性提高了1.5倍。另外,Tong等人通过对T. leycettanus的SBD区域进行替换修饰和定点突变,开发了三个活性、分泌和产量均提高的葡萄糖淀粉酶突变体,其中突变体TlGA-M7表现出最高的表达水平和对生玉米淀粉的有效水解。
有趣的是,SBD内的淀粉结合位点可能通过破坏生淀粉结构或吸附/结合到生淀粉颗粒上来影响酶的催化效率。地衣芽孢杆菌α-淀粉酶BliAmy中两个SBD残基的双突变使其生淀粉结合能力至少减弱了5.5倍。相反,有报道显示来自Photobacterium gaetbulicola的突变体AmyPG-SBDK626A和AmyPG-SBDT618A表现出更强的破坏能力和增强的生淀粉水解活性⁹⁴。此外,SBD中带有羰基的残基被认为能增强与淀粉的结合活性,从而提高来自米根霉的葡萄糖淀粉酶RoGA的降解能力。
通过遗传操作进行N/C末端和SBD工程改造N端或C端提供了一条快速、结构极简的途径,可以在不改变核心折叠的情况下调节底物结合、催化效率和胁迫耐受性。例如,GH13_45亚家族的α-淀粉酶通常具有一个独特且保守的C端区域,以来自巨大芽孢杆菌NL3的RSDA BmaN1为例,该区域显著增强了BmaN1对生淀粉的结合亲和力及其降解生淀粉颗粒的能力。类似地,来自嗜热脂肪地芽孢杆菌的RSDA Gt-amy通过其CTD结合生淀粉,该结构域也有助于维持其热活性和稳定性。相反,BaqAΔC中C端34个氨基酸的缺失赋予海洋芽孢杆菌显著的耐盐性,并在高盐条件下增强其淀粉分解活性。
SBD通过决定酶对颗粒淀粉的亲和力,独立地调控生淀粉水解。去除来自嗜酸乳杆菌NCFM普鲁兰酶的N端CBM41,会将有效攻击位点的密度降低,并使与玉米淀粉颗粒的结合减弱10倍。因此,将SBD融合到淀粉降解酶的N端或C端,有望增强其与完整淀粉颗粒的相互作用。与这一预期一致,来自南极细菌Pseudoalteromonas haloplanktis TAB23的冷适应α-淀粉酶通过一个十肽与黑曲霉葡萄糖淀粉酶的SBD或拟南芥葡聚糖-水二激酶3的SBD进行C端连接。由此产生的嵌合体AHA-SBDGA和AHA-SBDGWD3,对颗粒淀粉的活性相较于原始酶提高了三倍,而界面动力学显示,有效攻击位点密度增加了五倍,结合位点密度增加了七倍。
类似地,大麦α-淀粉酶AMY1通过一个37残基的连接肽与黑曲霉葡萄糖淀粉酶GA-I的C端SBD融合后,对淀粉颗粒的活性显著提高。将来自Cryptococcus sp. S-2 α-淀粉酶的SBDC端融合到AmyP的C端,其重组RSDA AmyP-C对生大米淀粉的催化活性提高了3.6-4.0倍,同时伴随着吸附能力和颗粒破坏能力的增强。最后,将CBM20与黑曲霉α-淀粉酶的N端融合,产生了嵌合酶CBM20_GH13,其对生马铃薯淀粉表现出优异的催化效率。
(2)遗传修饰策略
基于对RSDEs结构和功能的理解,采用遗传修饰来增强酶的性能、产量和活性。目前的研究集中于优化目标基因的密码子、增加基因拷贝数、选择合适的启动子、共表达分子伴侣以及优化蛋白质分泌途径。
用于转录增强的启动子工程通过精确调整启动子强度和转录起始效率,启动子工程作为最大化重组蛋白产量的首要(且通常是限速的)杠杆。一种新型RSDA AmyZ1在枯草芽孢杆菌中表达,通过构建改良的双启动子系统并优化5'-近端编码序列,在摇瓶中实现了1691.1 U/mL的酶活,在3 L发酵罐中达到了14,012 U/mL。相反,Yao等人通过顺序优化各种遗传元件和发酵培养基,获得了菌株WBZ-VY-B-R1,在摇瓶条件下酶活达到5733.5 U/mL,据报道这是重组RSDA的最高记录(此时枯草芽孢杆菌的OD600大于5.0)。在本实验室,Wang等人使用强启动子pPoxEgCel5B和信号肽spPoxGA15A,在草酸青霉中过表达了关键的RSDE基因PoxGA15A。在此情况下,突变菌株OXPoxGA15A的RSDE产量达到241.6 U/mL。目前,本实验室的RSDE产量已达到510.9 U/mL。此外,研究表明,启动子近端内含子可以增强酿酒酵母中的RSDE活性。
密码子优化与多拷贝基因整合密码子优化与多拷贝整合相结合,可同时提高翻译效率和基因剂量,为高水平异源蛋白生产提供了一条直接、染色体稳定的途径。Cripwell等人将从Talaromyces emersonii来源的经密码子优化的RSDG基因TemG_Opt与其内源α-淀粉酶基因temA组合,整合到具有淀粉分解能力的工业酿酒酵母菌株Ethanol Red和M2n中。重组菌株ER T12和M2n T1通过一步发酵工艺,能有效地将生玉米淀粉转化为乙醇。其中,表现优异的菌株ER T12在32°C下进行96小时的整合生物加工发酵后,达到了理论乙醇产率的93%。此外,将两个拷贝的来自扣囊复膜孢酵母的密码子优化的RSDG基因整合到工业酵母菌株酿酒酵母CCTCC M94055的基因组中。所得基因改造菌株CIBTS1522,在工业应用中发酵生玉米或生木薯淀粉时,所需的葡萄糖淀粉酶剂量至少减少了30-40%。
用于分泌或稳定性的融合蛋白策略此外,将分泌信号、稳定结构域、亲和标签和目标酶组合到一个开放阅读框中,可以同时提高分泌效率、酶性能和纯化回收率,提供了一种基因层面的模块化捷径,以实现更高的胞外酶产量和延长的催化活性,同时降低下游成本。例如,新型功能单元的融合或外部基因的整合可以提升目标蛋白的表达水平和产量。类似地,嵌合酶也被设计用于提高稳定性和改变底物或产物偏好。例如,来自Bacillus acidicola的嵌合α-淀粉酶与来自黑曲霉的RSDG融合,产生了酶Amy-Glu,该酶在4小时内转化了45%的生小麦淀粉和40%的生玉米淀粉,降解效率提高。需要注意的是,SBD的引入、删除或定点突变是通过遗传操作完成的,因此也构成了一种基因层面的融合蛋白修饰。
用于高产生淀粉降解酶的基因工程菌株构建
提高RSDEs产量的常见策略主要包括优化发酵工艺和进行基因工程改造。发酵优化主要涉及控制菌丝形态、调整培养基和发酵参数,以及利用限氧条件。在限氧条件下,更多的前体物质(如氨基酸)被重新导向用于酶的生产,从而提高酶产量。目前,正在开发基因工程菌株以提高同源表达和分泌效率,从而降低工业应用成本。
(1)基于诱导糖浓度变化的基因工程
减少由α-葡萄糖苷酶的转糖苷作用引起的非诱导糖(包括异麦芽三糖和潘糖)的积累,对于提高葡萄糖淀粉酶活性至关重要。例如,Guo等发现,在agdA/agdB双敲除菌株中过表达α-葡萄糖苷酶的B-P1结构域,显著提高了葡萄糖淀粉酶活性并减少了转糖基化产物。相反,胞内α-葡萄糖苷酶MalT将麦芽糖转化为异麦芽糖(作为一种强诱导糖),从而激活AmyR表达并促进淀粉水解。
(2)基于调控因子和酶基因表达变化的基因工程
首先,近期关于丝状真菌酶表达的基因工程研究集中于修饰调控网络。研究工作包括敲除负调控因子和过表达或组合表达正调控因子或酶。例如,在黑曲霉中过表达NADH激酶基因AN17和苹果酸酶基因maeA,使葡萄糖淀粉酶产量提高了90%。在重组黑曲霉中过表达amyA和葡萄糖淀粉酶基因glaA,并结合酪蛋白磷酸肽,显著增强了葡萄糖淀粉酶的表达和分泌。整合了来自泡盛曲霉的葡萄糖淀粉酶基因和来自Debaryomyces oceentalis的α-淀粉酶基因的酿酒酵母,能够提高RSDE产量,并发酵20%(w/v)的生玉米淀粉,产生10.3%(v/v)的乙醇。Cripwell等人在工业菌株ER T12中过表达了经密码子优化的TemG_Opt基因,导致了更高的生淀粉转化率和36%的乙醇浓度提升。此外,所得重组菌株ER T12.7能够从稻米废弃物中顺序生产生物乙醇和生物甲烷。
Zhao等人通过在草酸青霉114-2菌株中过表达AmyR和非组蛋白染色体蛋白HepA、敲除CreA以及激活G蛋白α亚基PGA3,进一步提高了RSDE产量。转录组分析显示这四个调控因子之间存在级联调控机制。在本实验室,基于草酸青霉HP7-1菌株,通过将PoxRsrA置于组成型启动子Ptef1控制下构建了过表达菌株OPoxRsrA,在可溶性玉米淀粉诱导2-4天后,其RSDE和可溶性淀粉降解酶产量提高了30.0-61.6%,证明了转录因子PoxRsrA作为提高RSDE产量靶点的潜力。随后,通过结合随机诱变和基因工程,在提高RSDE产量方面取得了显著进展。菌株OXPoxGA15A经过多轮常压室温等离子体、甲基磺酸乙酯和Co60-γ射线辐照诱变。在此基础上,研究人员敲除了淀粉酶阻遏基因cxrC并过表达了激活基因amyR,构建了工程菌株GXUR001,该菌株产生252.6 U/mL的RSDE,并在120小时后对150 g/L生木薯淀粉的葡萄糖转化率达到93.0%。
此外,高产RSDE工程菌株的理性人工设计已经广泛应用。例如,将Xln R的DNA结合区域替换为AmyR的相应区域,构建了人工转录因子AXTF。随后将该因子整合到构巢曲霉的AmyR缺陷突变株SA1中,获得了菌株AXTF。在以木糖或稻草水解液为碳源培养时,AXTF菌株产生了超过590 U/mL的α-淀粉酶和362 U/mL的α-葡萄糖苷酶。
(3)基于代谢途径改变的基因工程
氨基酸生物合成可以有效缓解葡萄糖淀粉酶生产中的氨基酸限制。例如,Cao等鉴定出丙氨酸、谷氨酸、甘氨酸和天冬氨酸是限制黑曲霉中葡萄糖淀粉酶合成的关键前体。在突变菌株OE-asp2中过表达天冬氨酸氨基转移酶基因,增强了胞内天冬氨酸水平和其他受限氨基酸前体的水平,显著提高了葡萄糖淀粉酶的产量。类似地,过表达参与脂肪酸降解的fadE和fadA基因,显著增加了胞内氨基酸库,并促进了葡萄糖淀粉酶的过量生产。NADPH的供应是氨基酸合成的一个限制因素。Sui等人过表达6-磷酸葡萄糖酸脱氢酶基因或maeA基因,使胞内NADPH库分别增加了45%和66%,导致葡萄糖淀粉酶产量分别提高了65%和30%。
此外,Zhu等人通过改造四个靶点并过表达Mtamy1和Mtpga3,构建了一株高产葡萄糖淀粉酶菌株MtGM12。其总分泌蛋白水平比野生型MtWT高出35.6倍,淀粉酶活性增加了51.9至55.5倍。在ΔracA菌株中,过表达葡萄糖淀粉酶基因glaA导致高尔基体后载体在菌丝尖端积累,从而使葡萄糖淀粉酶GlaA的分泌增加了四倍。这一发现证实了菌丝尖端的数量对蛋白质分泌有积极影响。通过代谢工程,在最适工程酵母菌株R23中过表达关键的内质网应激耐受基因HMO1并敲除BIO5,在用衣霉素处理时,α-淀粉酶产量提高了2.14倍。协同地删除/下调与过表达未折叠蛋白反应信号通路相关的基因,可以显著提高工程酵母菌株中的蛋白质分泌,使α-淀粉酶产量增加3.3倍。
RSDEs在各行各业的应用
在降低的温度下彻底分解含淀粉原料可以降低能耗和运营成本。RSDEs的应用主要集中在几个关键领域,包括食品加工、能源生产(如乙醇发酵)、化学工业以及多孔淀粉等生物材料的制备。
(1)冷水解甜味剂、饮料和饲料:提升碎米、木薯和其他低价值农作物的附加值
RSDEs可用于生产各种淀粉糖浆。例如,来自一种新型淀粉转化细菌Priestia koreensis HL12的酶,可以充分地将非热处理的木薯浆转化为麦芽低聚糖。随后,这些糖浆可以发酵成酒精、烈酒、米酒、醋和乳酸。此外,RSDEs还能直接水解碎米、糙米和黑米以生产糖浆、酒、醋和细菌纤维素,显著提升了低成本农作物的价值。例如,使用250 g/L的碎米作为底物,可以生产含5.4%乙酸的醋。此外,从糙米和黑米中提取的125 g/L糖溶液可用于制造细菌纤维素,这是一种适用于食品和化妆品领域的新型健康产品。RSDEs还能使非淀粉分解型微生物利用淀粉来生产乳酸。
此外,在动物饲料中添加RSDEs可以提高其营养价值,改善消化效率,并有助于分解抗营养因子,从而促进动物生长。解淀粉类芽孢杆菌菌株A17能够在烤烟叶片表面产生RSDEs,从而降低烟叶中的淀粉含量,并增加甜味和果味香气化合物的存在。来自枯草芽孢杆菌S113的钙非依赖型酸性RSDA能完全降解生小麦和生马铃薯淀粉,主要应用于烘焙行业。
(2)节能型燃料乙醇:生木薯的高浓SSF与重组酵母系统
同步糖化发酵将RSDEs的酶促淀粉消化与葡萄糖的乙醇发酵结合起来,从而节省了高温淀粉糊化的能量并降低了成本。在SSF中使用耐热酵母菌株,可以维持既能支持酶效力又能进行酵母发酵的温度。因此,SSF在乙醇生产中的应用已被广泛探索和推进。值得注意的是,利用RSDEs降解生木薯淀粉生产燃料乙醇已引起广泛关注和实际应用,其在乙醇产量和发酵特性方面与玉米淀粉相当。例如,通过基因工程和随机诱变获得了一株高产RSDEs的草酸青霉突变株GXUR003。当使用280 g/L生木薯淀粉为底物,添加40 U/g的粗RSDEs,并补充商业α-淀粉酶和葡萄糖淀粉酶进行SSF时,乙醇产量达到111.6 g/L,对应高达14.2%(v/v)的浓度。
此外,Cripwell等人专注于通过使用高产RSDG的重组酵母菌株提高乙醇发酵效率,特别是在将生淀粉转化为乙醇方面,为更可持续和更具成本效益的生物燃料生产过程做出了贡献。有趣的是,马克斯克鲁维酵母作为工业乙醇生产中酿酒酵母的潜在替代品,已广泛应用于乙醇发酵,其与RSDEs的协同作用可以显著降低能耗并提高生产效率。例如,在马克斯克鲁维酵母菌株YRL 009的最适发酵温度42°C下,使用200 g/L的生木薯淀粉为底物,乙醇产量可达66.52 g/L。
(3)更环保的纺织退浆、洗涤增效剂和纸张增强:碱性与固定化RSDEs
在化学工程领域,将碱性RSDEs添加到商业洗涤剂中可以提高棉织物的洗涤效率。来自Paenibacillus lactis OPSA3的一种新型RSDA已永久附着在用戊二醛活化的银纳米颗粒上,与未固定的酶相比,其储存稳定性和热稳定性显著提高,尤其是在暴露于普通清洁剂时。在纺织工业中,加入RSDEs有助于去除织物上的淀粉和杂质,从而提高其柔软度和光泽度。此外,RSDA的固定化处理进一步提高了退浆性能。在造纸生产中,添加RSDEs可以提高纸张的强度和光滑度,研究表明葡萄糖淀粉酶在再生纸的生物漂白中起着重要作用。
(4)定制化多孔淀粉:食品活性成分的包埋载体、药物递送系统及水处理吸附剂
RSDA和RSDG是制备多孔淀粉时常用的酶。多孔淀粉在食品工业中有广泛的应用,可作为着色剂、香料、调味料、多酚、精油、益生菌和甜味剂的载体。它们还有助于保护敏感成分,如油脂、矿物质、维生素、生物活性脂质以及β-胡萝卜素和番茄红素等食品色素,这些成分容易受光照、氧化或高温的影响。此外,具有不同孔结构的多孔淀粉在药物递送系统、吸附剂和生物传感器方面具有潜在应用。例如,多孔淀粉因其高比表面积和优异的吸附性能,可以有效地吸附和去除水处理中的染料污染物和重金属离子。
未来发展与展望
RSDEs及其工程菌株的开发已进入关键阶段。尽管传统的酶工程和代谢优化策略已显著提高了催化效率和产量,但持续的进步现在需要范式转变——从渐进式改进转向集成化、智能化和以应用为导向的设计。合成生物学、机器学习、系统生物学和纳米材料等新兴技术正在催化整个RSDE流程的变革性方法:从从头发现和计算机酶设计,到先进的异源表达平台和用于协同催化的工程化多酶系统。此外,解码复杂的基因调控网络为理性重编程细胞工厂开辟了新途径,而可持续性原则的整合则将RSDEs的应用范围扩展到循环生物经济领域。未来的关键方向包括以下几点。
智能酶挖掘与计算机设计宏基因组学、基于CRISPR的功能筛选和深度学习模型的融合,正在改变RSDEs的发现方式。这种协同方法加速了新RSDEs的鉴定,并能可靠地计算机预测其催化活性、底物特异性和结构稳定性,显著减少了对劳动密集型实验筛选的依赖。未来的工作应扩展分子工程策略,以进一步提升RSDEs的性能,为工业和生物工程应用中的卓越生物催化剂铺平道路。
先进的异源表达平台从传统宿主转向工程化的非模式微生物——如耐胁迫酵母和高分泌丝状真菌——为当前在产量、可放大性和工艺稳健性方面的瓶颈提供了有前景的解决方案。优化宿主-酶兼容性和分泌途径对于实现工业化规模的高效生产至关重要。利用系统生物学和生物信息学分析大规模基因表达数据,将进一步支持表达系统的理性设计,实现稳定、高水平的RSDEs合成。
用于协同催化的工程化多酶系统超越单一酶的应用,通过蛋白质支架构建或固定在纳米结构载体上的模块化多酶复合物,能够在环境温度下实现生淀粉的协同降解。这种空间组织优化了底物通道,提高了转化效率,并减少了总酶用量,为生物质利用提供了一种更节能、更具成本效益的方法。
通过解码调控机制理性工程化细胞工厂对基因表达调控的更深入理解对于工程化高产微生物菌株至关重要。阐明调控因子、信号通路和染色质重塑过程之间的相互作用,将揭示控制淀粉酶生产的关键机制。这些知识可以指导开发创新的调控工具和多层次控制策略——涵盖转录、转录后和表观遗传水平——实现对酶生物合成的精准操纵,提高生物技术产出。
拓展至可持续的工业应用除了生物燃料和食品加工,RSDEs在将富含淀粉的农业工业废弃物高值化利用方面也具有巨大潜力,例如将木薯皮和食物垃圾转化为生物塑料、益生元和增值化学品,或用于生物修复。实现这一潜力需要跨学科合作和工艺整合。展望未来,RSDEs有望推动可持续工业过程的创新,提高资源效率、环境保护和产品性能,横跨食品、化工、纺织和环境等领域。
总之,RSDEs的未来发展不在于孤立的性能优化,而在于系统层面的协同创新。只有深度融合酶的智能设计、细胞工厂的理性重工程和可持续生物过程工程,构建从分子发现到工业应用的一体化平台,才能推动生物技术迈向高效率、低碳、低废弃。这种系统范式不仅能提高淀粉资源的利用效率,还将加速生物基产品在食品、化工、材料和环境领域的大规模应用,为循环经济和绿色制造提供强大的技术支持。



 行业动态
行业动态